![]() Боли
Боли за грудиной могут подразумевать огромное количество заболеваний и патологических состояний, одновременная диагностика которых не под силу даже самому знающему врачу при условии наличия у него всех необходимых для этого средств. В связи с этим в первую очередь осуществляется исключение наиболее опасных для жизни заболеваний, связанных с патологией
сердца и легких. Затем, исключаются нагноительные процессы и злокачественные новообразования, и лишь после этого диагностируются оставшиеся заболевания, которые могут быть причиной появления такого симптома как
боль в груди.
Лечение заболеваний должно начинаться только после установления точного диагноза, однако на практике происходит несколько иначе. Процесс диагностики может затянуться на неизвестный период, в то время как состояние больного может стремительно ухудшаться. По этой причине в подобных случаях врачи вынуждены назначать лечение эмпирически (
интуитивно), основываясь на скудной информации, которой располагают на тот момент. Исход такого лечения может быть различным, поскольку, к сожалению, медицина наука не точная и не терпит аксиом.
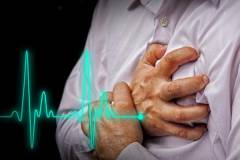
Боли за грудиной возникают при следующих заболеваниях: Боли за грудиной при ишемической болезни сердца (ИБС)
![]()
ИБС является патологическим состояниям, при котором потребности миокарда в кислороде превышают возможности его доставки.
Причины ишемической болезни сердца
Как правило, данное заболевание развивается по причине нарушения циркуляции крови по коронарным артериям при
атеросклерозе, тромбоэмболии, сосудистом спазме и др.
Симптомы ишемической болезни сердца
ИБС может протекать как бессимптомно, так и с яркими клиническими проявлениями. Бессимптомное течение характерно для некоторой части пациентов с многолетним течением
сахарного диабета, в то время как остальная часть больных ИБС испытывает такие симптомы как загрудинная боль,
одышка, сильное сердцебиение, нарушение сердечного ритма, головокружение (
снижение артериального давления), психомоторное возбуждение (
страх смерти) и т. д. Наиболее тяжелым исходом ИБС является острый инфаркт миокарда и внезапная смерть.
Диагностика ишемической болезни сердца
Определение дефицита кислорода и избытка продуктов метаболизма в миокарде осуществляется при помощи электрокардиограммы (
ЭКГ). Данный метод является основным и наиболее доступным в определении фаз инфаркта миокарда и
аритмий. Тем не менее, нужно помнить, что электрокардиограмма демонстрирует признаки ишемии (
недостаточное кровоснабжение ткани) миокарда только в 60 - 70% случаев.
Более точные данные при ИБС можно получить, применяя ЭхоКГ (
эхокардиография или ультразвуковое исследование сердца), совмещенное с доплером. Данное исследование позволяет обнаружить непосредственно участки нарушенного кровотока в коронарных артериях, а также участки миокарда с более слабым сокращением.
Коронарография или
ангиография коронарных артерий по праву считается самым точным исследованием, позволяющим определить локализацию сужения просвета коронарных артерий. Однако проведение данного исследования связано с определенными рисками, заключающимися в использовании контрастного вещества, способного у некоторых больных вызвать аллергическую реакцию. Кроме того, для данного исследования необходима пункция бедренной артерии и проведение специального зонда к устьям коронарных артерий, находящимся в восходящей аорте, позади створок аортального клапана сердца.
В силу того, что ИБС может иметь разнообразные проявления, используемые лабораторные анализы также могут разниться. Учитывая то, что при
стенокардии некроза миокарда не происходит, в крови следует искать признаки нарушения обмена веществ, ведущего к отложению атеросклеротических бляшек. Таким образом, при ИБС, вызванной атеросклерозом коронарных артерий, увеличивается уровень общего
холестерина, триглицеридов, липопротеидов низкой плотности, аполипопротеина А1 и В.
При инфаркте миокарда на фоне ИБС появляются признаки некроза сердечной мышцы, подтверждаемого лабораторно ростом уровня тропонинов (
I и T) в крови, креатинфосфокиназы (
в частности фракции МВ), лактатдегидрогеназы,
трансаминаз и миоглобина.
Необходимый специалист при ишемической болезни сердца
Электрокардиографические признаки ишемии и острого инфаркта миокарда известны врачу любой специальности. Однако более изощренные исследования доступны лишь в условии кардиологического стационара под наблюдением врача-кардиолога.
Методы лечения ишемической болезни сердца
Немедикаментозное лечение направлено на уменьшение физической нагрузки и массы тела. Снижение уровня жиров крови предотвращает развитие атеросклеротических бляшек.
Медикаментозное лечение подразумевает использование нескольких групп препаратов. Антиагреганты (
аспирин, клопидогрел и др.) предотвращают склеивание
тромбоцитов и
эритроцитов, улучшая таким образом реологические свойства крови и предотвращая формирование
тромбов.
Бета-адреноблокаторы (
метопролол, бисопролол, карведилол) снижают частоту сердечных сокращений и удлиняют диастолу (
пауза между сокращениями желудочков сердца), что уменьшает потребности миокарда в кислороде и улучшает его кровоснабжение.
Статины (
симвастатин, аторвастатин и др.) снижают уровень общего холестерина в крови и липопротеидов низкой плотности, предотвращая формирование атеросклеротических бляшек.
Нитраты (
нитроглицерин, изосорбида мононитрат) применяются с целью снятия приступов стенокардии путем расширения коронарных артерий, периферических вен и уменьшения таким образом преднагрузки на сердце.
Антикоагулянты (
гепарин, фраксипарин, варфарин и др.) снижают скорость формирования фибриновых нитей и ускоряют их разрушение, за счет чего вероятность формирования тромба значительно уменьшается, а уже сформированные тромбы постепенно рассасываются.
Мочегонные средства (
фуросемид, торасемид, индапамид) снижают артериальное давление путем выведения жидкой части крови и уменьшения ее объема. Вместе с этим снижается постнагрузка на сердце, что значительно снижает его энергетические затраты и предотвращает приступы стенокардии.
Антиаритмические препараты (
амиодарон, соталол, верапамил и др.) восстанавливают правильный сердечный ритм, нормализуя длительность диастолы и улучшая питание миокарда.
Ингибиторы АФП (
ангиотензинпревращающего фермента) (
лизиноприл, эналаприл, каптоприл) снижают системное артериальное давление и вместе с ним постнагрузку на сердце.
Загрудинные боли при остром инфаркте миокарда
![]()
Острый инфаркт миокарда является одним из наиболее неблагоприятных форм ИСБ, сущность которого заключается в некрозе (
омертвении) некоторого участка сердечной мышцы. Чем больше объем некротизированного участка, тем выраженнее дефицит сократительной функции сердца и тем фатальнее прогноз.
Причины инфаркта миокарда
Причинами острого инфаркта миокарда являются все патологические процессы, приводящие к нарушению равновесия между энергетическими потребностями миокарда и возможностями их обеспечения. В частности, некроз сердечной мышцы может развиться на фоне аритмии, длительного спазма коронарных артерий, тромбоэмболии коронарных артерий, миокардита, гипертрофии левых отделов сердца и др.
Симптомы инфаркта миокарда
Типичными симптомами острого инфаркта миокарда являются сильнейшие загрудинные давящие или жгучие боли, иррадиирующие (
отдающие) в левое плечо и руку, одышка, снижение артериального давления, бледность и синюшность кожных и слизистых покровов, сильные сердечные сокращения, головокружение, потеря сознания, страх смерти и др.
Однако следует упомянуть, что инфаркт миокарда может протекать совсем нетипично. В частности, боли могут ощущаться не за грудиной, а в плече, шее, нижней челюсти или животе. У больных сахарным диабетом инфаркты могут протекать совсем безболезненно, лишь с признаками нарушения гемодинамики.
Диагностика инфаркта миокарда
Диагностика инфаркта миокарда основывается на инструментальных и лабораторных исследованиях. Среди инструментальных методов следует выделить электрокардиограмму, эхокардиографию с доплером и коронарографию. На электрокардиограмме обнаруживаются признаки ишемии и некроза миокарда (
в различные стадии инфаркта). На эхокардиографии с доплером определяется проходимость наиболее крупных сегментов коронарных артерий, а также оценивается сократительная функция всех отделов миокарда. В области некроза тонус сердечной мышцы ослабевает, из-за чего она сокращается заметно слабее или не сокращается совсем. Коронарография при инфаркте миокарда способствует выявлению участков сужения коронарных артерий на всем их протяжении (
даже наиболее узкие ветви).
Лабораторная диагностика заключается в применении таких маркеров как тропонины, креатинфосфокиназа (
МВ фракция), лактатдегидрогеназа, трансаминазы, миоглобин и др. Также важно сделать
общий анализ крови с лейкограммой, поскольку через несколько часов после инфаркта отмечается прогрессирующее увеличение количества
лейкоцитов со сдвигом лейкоцитарной формулы влево.
Необходимый специалист при инфаркте миокарда
На начальных этапах острый инфаркт миокарда может диагностировать врач любой специальности, однако дальнейшее лечение должно осуществляться в кардиологическом стационаре под надзором кардиолога и при необходимости кардиохирурга.
Методы лечения инфаркта миокарда
Первая помощь заключается в придании больному полусидячего положения и освобождение воротниковой зоны. Необходимо позвать на помощь окружающих и вызвать бригаду скорой помощи. При наличии у больного таблеток нитроглицерина следует одну из них поместить под язык. Если боли не проходят, то через 5 - 7 минут следует дать еще одну таблетку. Если и на этот раз боли не проходят, то через очередные 5 - 7 минут можно дать третью – последнюю таблетку.
Врачебная помощь заключается в обезболивании (
морфин), введении антикоагулянтов (
гепарин, фраксипарин) и стабилизации гемодинамических показателей (
нормализация сердечного ритма и артериального давления).
В условиях стационара можно предпринять попытку разрушения тромба такими тромболитическими препаратами как урокиназа, стрептокиназа или альтеплаза. При наличии показаний к операции осуществляют аортокоронарное шунтирование, установку искусственных стентов и другие реконструктивные хирургические вмешательства.
Подпишитесь на Здоровьесберегающий видеоканал


Боли за грудиной при расслаивающей аневризме аорты
![]()
Расслаивающая аневризма аорты является патологическим состоянием, при котором в интиме (
внутренней оболочке) данного сосуда развивается дефект, через который в толщу стенки постепенно просачивается кровь. Из-за высокого давления кровь постепенно отделяет интиму от мышечной оболочки аорты или разрыхляет мышечную оболочку и адвентицию (
внешняя соединительнотканная оболочка аорты). В первом случае отслойка может достигнуть ветвей аорты и сузить их, приводя к недостаточному кровоснабжению соответствующих органов и тканей. При ретроградной отслойке (
в направлении к сердцу) может произойти кровотечение в перикард, тампонада сердца (
сдавление миокарда кровью), отсутствие эффективных сердечных сокращений и гибель больного. Во втором случае, кровь может просочиться через все слои аорты с развитием клиники острого внутреннего кровотечения, также приводящего к летальному исходу.
Причины развития расслаивающей аневризмы аорты
Основной причиной расслаивающей аневризмы аорты является выраженный атеросклероз и
гипертоническая болезнь. Сифилитический мезаортит и травмы грудной клетки также могут привести к развитию данной патологии, однако значительно реже. Причина этого кроется в том, что третичный
сифилис в последнее время встречается все реже, а травмы грудной клетки сами по себе часто приводят к гибели больных, таким образом, что осложнения не успевают развиться. Также в литературе описаны случаи расслаивающей аневризмы аорты при
сепсисе, врожденных
пороках сердца, инфильтрации опухоли в стенку аорты и др.
Симптомы расслаивающей аневризмы аорты
Основным симптомом является сильнейшая боль в области отслойки аорты (
брюшная полость, грудная полость, непосредственно позади грудины и др.), которая может иррадиировать (
отдавать) по ходу основных ветвей аорты (
сонные артерии, подключичные артерии и др.). В момент открытия внутреннего кровотечения (
прободение сосудистой стенки) или тампонады сердца отмечается резкое снижение артериального давления и учащение сердечных сокращений. Клиническая картина расслаивающей аневризмы аорты может развиваться как в течение нескольких часов, так и на протяжении нескольких недель. Чем медленнее прогрессирует отслойка интимы, тем большим временем располагают врачи для постановки диагноза и спасения жизни больного.
Диагностика расслаивающей аневризмы аорты
При появлении выраженных загрудинных болей в список причин в обязательном порядке следует включить и расслаивающую аневризму аорты. Подтверждение данного анализа осуществляется посредством непосредственной визуализации самой аневризмы. Визуализировать данные дефект аорты можно при помощи чреспищеводной эхокардиографии, а при ее отсутствии – посредством обычной трансторакальной эхокардиографии.
Отдельного внимания заслуживает аортография. При данном исследовании через одну из крупных периферических артерий, вводят зонд с гибким проводником. Далее, зонд проводят вплоть до начального сегмента восходящей части аорты, подают контрастное вещество и делают приблизительно по 1 - 2 рентгеновскому снимку в секунду на протяжении 5 - 10 секунд. Полученные изображения позволяют оценить особенности кровотока в данном сосуде и его ветвях. Однако, несмотря на все плюсы данного исследования, оно не всегда может быть показано при расслаивающей аневризме аорты в связи с тем, что зонд не всегда может пройти выше места отслойки, а также в связи с риском прободения и без того истонченной стенки аорты. Таким образом, к данному исследованию можно прибегнуть лишь в том случае, если остальные неинвазивные (
малотравматичные) способы визуализации недоступны.
Необходимый специалист при расслаивающей аневризме аорты
При подозрении на расслаивающую аневризму аорты следует в срочном порядке вызвать скорую помощь или самостоятельно обратиться в ближайшую больницу или кардиологический центр. Специалистом, занимающимся лечением данного острого состояния, является кардиохирург.
Методы лечения расслаивающей аневризмы аорты
На догоспитальном следует поддерживать систолическое артериальное давление больного в пределах 100 - 120 мм ртутного столба. Оптимальной частотой сердечных сокращений является 50 - 60 ударов в минуту. Достижение данных целевых показателей осуществляется при помощи нитроглицерина, бета-адреноблокаторов (
пропранолол, эсмолол и др.) и блокаторов кальциевых каналов (
верапамил, дилтиазем).
Ход дальнейшего лечения зависит от степени выраженности аневризмы и темпов ее прогрессии. Медикаментозное лечение возможно при небольших и стабильных аневризмах. При всех остальных аневризмах выполняется традиционное оперативное вмешательство или подведение стента через надрез в бедренной артерии и компрессия места отслойки.
Боли за грудиной при приступе пароксизмальной тахикардии
![]()
Пароксизмальная тахикардия представляет собой резко возникающее и, как правило, резко прекращающееся нарушение сердечного ритма, при котором частота сердечных сокращений достигает 140 - 240 ударов в минуту.
Причины возникновения пароксизмальной тахикардии
Нарушение сердечного ритма возникает в результате появления в любой части миокарда эктопического очага возбуждения. Если очаг находится в предсердиях, то такой вид пароксизмальной тахикардии называется наджелудочковым. Наджелудочковые тахикардии менее опасны в связи с тем, что часть импульсов блокируется предсердно-желудочковой перегородкой, в результате чего желудочки сокращаются в несколько раз реже, чем предсердия, и не происходит выраженных нарушений гемодинамики. В случае если очаг возбуждения находится в желудочках сердца, то такой вид пароксизмальной тахикардии называется желудочковым. Желудочковые тахикардии значительно опаснее для жизни, поскольку частота сокращения желудочков при них очень высока и вызывает выраженные нарушения гемодинамики и гибель больного.
Непосредственных причин возникновения в миокарде эктопических очагов возбуждения много. В частности, речь идет о нарушениях электролитного состава крови, повышении уровня катехоламинов, рубцовых постинфарктных изменениях, некоторых сопутствующих заболеваниях (
язвенная болезнь желудка и двенадцатиперстной кишки, приступ желчекаменной болезни, рефлюкс-эзофагит) и др.
Симптомы пароксизмальной тахикардии
Возникновение приступа пароксизмальной тахикардии, как правило, наступает резко и проявляется сильным и частым сердцебиением, загрудинными давящими болями, резкой
слабостью, головокружением, обильным потоотделением,
тошнотой и в некоторых случаях
рвотой. Кожные покровы становятся резко бледными. Шейные вены переполняются и пульсируют. Момент выхода из приступа также является четким, после чего состояние больного в течение нескольких минут восстанавливается.
Диагностика пароксизмальной тахикардии
Для того чтобы запечатлеть приступ пароксизмальной тахикардии, необходимо сделать электрокардиограмму в период клинического проявления приступа. Довольно часто данные приступы не удается засвидетельствовать, поскольку они самостоятельно завершаются до того как прибудет бригада скорой помощи. В связи с этим больным с подобными приступами рекомендуется делать электрокардиографию по Холтеру, суть которой заключается в ношении на поясе портативного электрокардиографа, который способен регистрировать электрическую активность сердца на протяжении нескольких суток. Использование данного аппарата позволяет не только зафиксировать приступы пароксизмальной тахикардии, но еще и способствовать в установлении диагноза других кардиологических заболеваний.
Необходимый специалист при пароксизмальной тахикардии
Диагностикой и лечением пароксизмальных тахикардий занимается кардиолог. При его отсутствии профилактику и лечение легких и среднетяжелых форм пароксизмальных тахикардий может осуществлять терапевт и семейный врач. Купированием приступов занимаются врачи скорой помощи.
Методы лечения пароксизмальной тахикардии
Методы лечения подразделяются на методы, направленные на купирование приступа, и методы поддерживающего лечения.
Для купирования приступа пароксизмальной тахикардии без наличия лекарственных веществ прибегают к так называемым вагусным пробам, призванным усилить влияние парасимпатической нервной системы и восстановить синусовый ритм. Наиболее распространенной пробой является проба Вальсальвы, суть которой заключается в глубоком вдохе, закрытии верхних дыхательных путей и натуживании, как при сильном выдохе. Помимо вышеуказанной пробы используется проба Даньини-Ашнера (
надавливание на глазные яблоки) и проба Геринга (
массирование мягких тканей в проекции бифуркации общей сонной артерии).
Препаратом выбора во время приступа пароксизмальной тахикардии является амиодарон (
кордарон). Преимущество данного препарата заключается в универсальности, поскольку он подходит для купирования как наджелудочковых, так и желудочковых тахикардий.
Поддерживающее лечение осуществляется противоаритмическими препаратами, нацеленными на предотвращение определенных видов аритмий, регистрируемых у конкретного больного. Также успешно используются препараты из группы бета-адреноблокаторов, блокаторов кальциевых каналов и сердечных гликозидов.
Боли за грудиной при остром перикардите
![]()
Перикардитом называется воспаление околосердечной сумки, сопровождающееся накоплением в ней серозной, серозно-геморрагической или гнойной жидкости и формированием фибриновых отложений. По причине утолщения стенки перикарда, а также из-за присутствия относительно большого количества жидкости в его полости происходит неполное расправление миокарда во время диастолы, из-за чего эффективность насосной функции сердца значительно снижается, а у больного проявляются признаки острой
сердечной недостаточности.
Причины развития острого перикардита
Причины перикардитов подразделяются на инфекционные и неинфекционные. К инфекционным поражениям сердечной сумки относятся бактериальные, вирусные, ревматические, грибковые и туберкулезные. К неинфекционным причинам относят атопические (
аллергические), травматические, лучевые (
пострадиационные), постинфарктные и метастатические.
Симптомы острого перикардита
В связи с тем, что перикардит может иметь различное клиническое течение и развиваться как осложнение большого числа заболеваний, типичные его симптомы перечислить достаточно сложно. Тем не менее, наиболее часто перикардит ассоциируется с синдромом общей интоксикации (
лихорадка, озноб, выраженная слабость), загрудинными болями ангинозного характера, увеличением частоты сердечных сокращений и признаками сердечной недостаточности (
прогрессирующие отеки нижних конечностей, одышка смешанного типа, акроцианоз и др.). В качестве дополнительных клинических признаков могут выступать симптомы основного заболевания, на фоне которого развился перикардит.
Диагностика острого перикардита
Для постановки такого диагноза необходимо четко визуализировать внешнюю оболочку сердца, оценить ее толщину и плотность, а также определить количество жидкости в перикардиальной полости. Все из вышеперечисленных задач выполняются при эхокардиографии. При помощи электрокардиографии можно лишь предположить наличие перикардита (
ишемические изменения, а также снижение вольтажа зубца R во всех отведениях).
Необходимый специалист при остром перикардите
Диагноз перикардит сможет выставить врач-кардиолог или терапевт при наличии соответствующих данных эхокардиографии. При необходимости пункции перикардиальной полости и изъятия находящейся в ней жидкости прибегают к помощи кардиохирурга.
Методы лечения острого перикардита
Консервативные методы лечения подразумевают компенсацию основного заболевания, на фоне которого развился перикардит (
антибиотики, противогрибковые, глюкокортикостероиды и др.). Патогенетическое лечение подразумевает использование мочегонных средств для уменьшения количества перикардиальной жидкости и средств, нормализующих гемодинамику. При констриктивном перикардите эффективным является только хирургическое лечение.
Боли за грудиной при инфекционном эндокардите
![]()
Инфекционный эндокардит является воспалительным заболеванием эндокарда (
внутренней оболочки сердца), при котором в патологический процесс вовлекается клапанный аппарат сердца, а также внутренние структуры желудочков и предсердий, являющиеся производными эндокарда (
сухожильные нити, хорды и др.). В результате, возникают приобретенные пороки сердца, обуславливающие развитие сердечной недостаточности различной степени выраженности. Помимо вышесказанного на клапанах сердца развиваются специфические наросты, называемые вегетациями, которые способны отрываться и мигрировать в сосудистое русло, вызывая системную тромбоэмболию.
Причины развития инфекционного эндокардита
Согласно данным последних исследований по изучению природы инфекционного эндокардита считается, что данное заболевание не развивается на интактных (
здоровых, неповрежденных) клапанах. Для развития воспаления необходимо, чтобы определенный участок эндокарда был поврежден (
субэндокардиальный инфаркт миокарда, механическое раздражение искусственными водителями ритма или искусственными клапанами, поражение клапанного аппарата антителами при ревматической лихорадке и др.).
Вторым условием развития инфекционного эндокардита является бактериемия – циркуляция в периферической крови патогенных микроорганизмов, очагом которых может быть любой хронический воспалительный процесс (
инфекции полости рта и носа, фурункулы, дерматиты, дивертикулы кишечника, остеомиелит и др.). Когда данные возбудители оседают на поврежденных участках эндокарда (
чаще это клапаны сердца) в них развивается воспаление. Спектр патогенных агентов, вызывающих воспалительный процесс, велик. Наиболее часто инфекционный эндокардит развивается при
стрептококковом поражении, более редкими возбудителями могут быть
стафилококки, энтерококки, синегнойная палочка, некоторые
вирусы, простейшие, грибы и др.
Симптомы инфекционного эндокардита
Для инфекционного эндокардита характерен полиморфизм клинической картины. Наиболее ранние признаки заболевания относятся к токсико-инфекционному синдрому (
затяжная лихорадка или субфебрилитет, выраженная общая слабость, обильное потоотделение и др.), возникновение которого редко удается связать с сердечной патологией. Признаки сердечной недостаточности появляются, когда развивается поражение клапанного аппарата сердца. Первым симптомом, свидетельствующим о сердечной недостаточности, является стойкое увеличение частоты сердечных сокращений, которое часто интерпретируется неверно. Далее, присоединяется одышка, отеки ног, синюшность кожных покровов, загрудинные боли и др.
В связи с тем, что при инфекционном эндокардите на поверхности клапанов образуются вегетации (
наросты), которые способны отрываться и вызывать тромбоэмболии периферических артерий, к вышеперечисленным симптомам присоединяются симптомы тромбоэмболий основных ветвей аорты. При попадании тромба в почечные артерии развивается клиника
гломерулонефрита (
поясничные боли, покраснение мочи). При закупорке печеночной артерии развивается клиника острой
печеночной недостаточности (
желтуха). При тромбоэмболии артерий головного мозга развивается клиника ишемического инсульта головного мозга (
частичный или полный паралич, нарушение речи, мышления, слуха, зрения и др.). Тромботическая закупорка капилляров проявляется геморрагической сыпью, формированием узелков Ослера (
небольшие болезненные уплотнения на ладонях), а также поражением сосудистой сети сетчатки глаз.
Сопутствующая
анемия, возникающая из-за разрушения эритроцитов при прохождении через стенозированные (
суженные) отверстия клапанов сердца, придает кожным покровам бледную окраску. Повышение фракции свободного
билирубина из-за разрушения эритроцитов окрашивает
кожу в характерный цвет «кофе с молоком».
Диагностика инфекционного эндокардита
Диагностика инфекционного эндокардита осуществляется на основе больших и малых критериев Дьюка. Большим критерием является положительная гемокультура (
выявление в крови патогенных бактерий путем посева на питательные среды) и визуализация поражения эндокарда (
вегетации, околоклапанный абсцесс) на ЭхоКГ.
К малым критериям относится наличие предрасполагающих факторов (
использование внутривенных наркотических средств, клапанные дефекты),
температура тела более 38 градусов на протяжении длительного времени, сосудистые феномены (
тромбоэмболии периферических артерий, геморрагическая сыпь, внутримозговые кровоизлияния), иммунные феномены (
гломерулонефрит, повышенный уровень ревматоидного фактора) и серологическое подтверждение активного инфекционного процесса.
Диагноз считается подтвержденным, если у больного присутствуют два больших критерия, один большой и два малых или пять малых критериев.
Необходимый специалист при инфекционном эндокардите
Диагностикой и лечением инфекционного эндокардита занимается кардиолог и при необходимости кардиохирург.
Методы лечения инфекционного эндокардита
Основа лечения заключается в уничтожении очага инфекции, расположенного в эндокарде. Выбор средств борьбы с возбудителем зависит от его природы. Подавляющее большинство случаев инфекционного эндокардита лечится применением комбинации из двух, трех и четырех антибиотиков. Реже используются противогрибковые и
противовирусные средства.
Боли за грудиной при синдроме Дресслера
![]()
Синдром Дресслера (
постинфарктный синдром) является аутоиммунным процессом, поражающим ткани сердца, легких и крупных суставов в период от 2-х до 6-ти недель с момента инфаркта миокарда. Типичными проявлениями являются перикардит, пневмонит,
плеврит и
артрит.
Причины развития синдрома Дресслера
Причины возникновения данного осложнения неизвестны, однако наиболее аргументированной версией на сегодняшний день считается аутоиммунная природа поражения.
Клинические проявления синдрома Дресслера
Классическими симптомами, отмечающимися при синдроме Дресслера, являются загрудинные боли, одышка, отеки ног, боли в области ребер, а также
боли и отечность крупных суставов.
Диагностика синдрома Дресслера
Диагностика данного синдрома основывается на данных анамнеза (
время, прошедшее с момента инфаркта миокарда), клинических проявлениях, а также подтверждении поражения легких и сердца на рентгенографии,
компьютерной томографии или эхокардиографии.
Необходимый специалист при синдроме Дресслера
Заподозрить развитие данного заболевания может кардиолог, пневмолог, ревматолог, терапевт или семейный врач, однако окончательной диагностикой и лечением его должен заниматься кардиолог.
Методы лечения синдрома Дресслера
Основой лечения являются глюкокортикостероиды, в частности, преднизолон в стартовой дозе 30 - 40 мг/кг.
Боли за грудиной при остром миокардите
![]()
Острый миокардит представляет собой воспаление мышечной оболочки сердца.
Причины острого миокардита
Наиболее часто миокардит развивается под воздействием вирусов. Различают также бактериальные, грибковые, аллергические и ревматические миокардиты. Значительную долю занимают идиопатические миокардиты, причин которых либо не обнаружено, либо чересчур много, и поэтому выбрать какую-то одну не представляется возможным.
Симптомы острого миокардита
Симптомокомплекс миокардита включает в себя проявления острого инфекционного синдрома (
температура, озноб, выраженная слабость, обильное потоотделение) и сердечной недостаточности (
отеки ног, акроцианоз, одышка, аритмии, загрудинные боли ангинозного характера и др.).
Диагностика острого миокардита
Для подтверждения миокардита следует выполнить рентгенографию в прямой и боковой проекции, электрокардиограмму и эхокардиографию. Если в достоверности диагноза остаются сомнения, то прибегают к более специфическим и дорогостоящим исследованиям (
магнитно-резонансная томография с мечеными антителами к актомиозину, эндокардиальная биопсия, определение генома вируса и серологическое исследование).
В подтверждение миокардита на рентгенограмме отмечается значительное увеличение границ сердца. На электрокардиограмме часто присутствуют предсердные и желудочковые экстрасистолы, нарушение процессов реполяризации, а также переходящие ишемические изменения, которые в совокупности со снижением амплитуды зубца R чаще в правых отделах сердца могут быть ложно интерпретированы как инфаркт миокарда. Эхокардиография при миокардите выявляет расширение полостей сердца, снижение сократительной функции миокарда, снижение насосной функции сердца.
Магнитно-резонансная томография с мечеными антителами к миозину выявляет очаги повреждения и некроза миокарда. Биопсия сердечной мышцы является достаточно сложной процедурой и часто дает противоречивые результаты, однако в некоторых случаях позволяет исключить более редкие заболевания и остановиться на диагнозе миокардита. Определение генома вируса, вызвавшего миокардит, осуществляется при помощи лабораторного исследования под названием
ПЦР (полимеразная цепная реакция). При серологическом исследовании определяется рост титра антител к данному вирусу в 4 и более раз.
Необходимый специалист при остром миокардите
Диагностикой и лечением миокардитов должен заниматься исключительно кардиолог.
Методы лечения острого миокардита
Лечение миокардита должно быть ориентировано на устранение вызвавшего его возбудителя. При вирусных миокардитах назначается противовирусная терапия и
нестероидные противовоспалительные средства. При бактериальных миокардитах назначаются антибиотики в комбинациях. При грибковых миокардитах назначаются противогрибковые средства. При аутоиммунных миокардитах выраженный эффект отмечается при использовании глюкокортикостероидной терапии.
Важнейшим условием, вне зависимости от выбранного медикаментозного лечения, является строгий постельный режим. При необходимости может применяться кислородная терапия.
Загрудинные боли при аневризме грудной аорты
![]()
Аневризмой грудной аорты называется локальной увеличение диаметра данного кровеносного сосуда в области грудного отдела нисходящей части аорты. Аневризмы грудной аорты могут быть расслаивающими и простыми. Расслаивающие аневризмы развиваются вследствие нарушения целостности внутренней оболочки данного сосуда и часто приводят к гибели больного. Простые аневризмы менее агрессивны и долго могут оставаться бессимптомными, однако периоды их роста могут сопровождаться загрудинными болями ангинозного характера. Помимо риска разрыва аневризмы, существует также высокая вероятность формирования тромботических масс в ее просвете, которые впоследствии могут приводить к системным тромбоэмболиям.
Причины аневризмы грудной аорты
Расслаивающие аневризмы грудной аорты развиваются чаще из-за выраженных атеросклеротических изменений и гипертонической болезни. Более редкой причиной является воспаление артериальной стенки при третичном сифилисе. Простые аневризмы грудной аорты развиваются в основном из-за врожденного дефекта ее стенки и могут достигать внушительных размеров, оказывая давление на соседствующие органы и анатомические структуры.
Симптомы аневризмы грудной аорты
Расслаивающая аневризма аорты характеризуется сильнейшими загрудинными болями, плохо поддающимися купированию. При ее разрыве возникает клиника геморрагического шока из-за массивного внутреннего кровотечения. Простые аневризмы длительное время никак не проявляются, за исключением чувства сильной пульсации в груди, однако периоды ее роста могут отмечаться легкими и умеренными болями в проекции аневризмы, которые усиливаются при повышении артериального давления и проходят при его нормализации. Гемодинамические нарушения при простой аневризме практически всегда отсутствуют.
Диагностика аневризмы грудной аорты
Аневризма значительных размеров может быть обнаружена при рядовой рентгенографии грудной клетки. Более точные данные о размерах и структуре аневризмы грудной аорты можно получить при эхокардиографии, аортографии, компьютерной томографии или магнитно-резонансной томографии с внутривенным контрастированием.
Необходимый специалист при аневризме грудной аорты
Специалистом, занимающимся выявлением и лечением аневризм грудной аорты, является кардиолог и кардиохирург.
Методы лечения аневризмы грудной аорты
Методы лечения всецело зависят от вида аневризмы и скорости ее прогрессии. Расслаивающие аневризмы грудной аорты необходимо лечить путем установки искусственного стента или путем открытой операции, прогноз которой чаще неблагоприятен.
Боли за грудиной при болезни Такаясу
![]()
Под болезнью Такаясу подразумевается аутоиммунное воспаление аорты и ее ветвей, проявляющееся формированием в ее стенке фиброзных гранулем, препятствующих току крови и приводящих к ремоделированию аорты с формированием на ее протяжении многочисленных аневризм.
Причины болезни Такаясу
Этиология данного заболевания неизвестна, как неизвестна этиология большинства системных аутоиммунных заболеваний.
Симптомы болезни Такаясу
Первым признаком болезни Такаясу является незначительное повышение температуры тела, в среднем, до 37,5 градусов. Может проявляться общая слабость, сохраняющаяся месяцы подряд. В связи с постепенным дебютом больные не придают большого значения вышеперечисленным изменениям. У части из них клинические проявления на первых стадиях болезни могут отсутствовать совсем. Лишь при выраженном ремоделировании аорты присоединяются загрудинные боли, вызванные ишемией гипертрофированного миокарда и ростом многочисленных аневризм.
Диагностика болезни Такаясу
Диагностика данного заболевания сводится к визуализации гранулем в стенке аорты, утолщения стенки аорты и ее ветвей, а также аневризм при выполнении эхокардиографии, аортографии, КТ или МРТ с сосудистым контрастированием.
Лабораторные анализы обладают невысоким процентом специфичности, поэтому они должны оцениваться лишь в совокупности с остальными клиническими и параклиническими данными. В общем анализе крови и в
биохимическом анализе крови присутствуют общие признаки воспаления, снижение уровня альбумина, гаптоглобина, холестерина и липопротеидов, а также увеличение уровня иммуноглобулинов и наличие HLA-антигенов. Биопсия аортальной стенки выявляет наличие в ней специфических гранулем, однако практически никогда не выполняется, в связи с высокой опасностью разрыва данного крупного сосуда.
Необходимый специалист при болезни Такаясу
Специалистом, занимающимся диагностикой и лечением данной патологии, является кардиолог, ревматолог и при необходимости кардиохирург.
Методы лечения болезни Такаясу
Основное лечение заключается в долговременной гормональной терапии. Начальной дозой преднизолона является 1 мг/кг в сутки. При непереносимости таких высоких доз гормонов их дозу постепенно уменьшают до комфортных для пациента значений.
Боли за грудиной при тромбоэмболии легочной артерии
![]()
Под тромбоэмболией легочной артерии подразумевается патологическое состояние, вызванное закупоркой легочной артерии и ее ветвей тромботическими массами.
Причины развития тромбоэмболии легочной артерии
В большинстве случаев тромбы формируются в венах нижних конечностей при
варикозном их расширении и реже в венах рук и правых отделах сердца. Также закупорка легочных артерий может осуществляться газами (
при кессонной болезни), амниотическими водами (
при обильных родовых кровотечениях) и жировыми эмболами (
при открытых костных переломах).
Симптомы тромбоэмболии легочной артерии
Клинические проявления зависят от калибра артерии в месте закупорки и от времени, прошедшего с начала тромбоэмболии.
В первые минуты после тромбоэмболии больной может ощущать одышку, сильное головокружение из-за резкого снижения артериального давления, слабость, давящие загрудинные боли. Кожные покровы становятся влажными, липкими и холодными, их цвет из бледно-розового становится бледно-синюшным. Спустя некоторое время может отмечаться повышение температуры тела.
При тромбоэмболии небольших ветвей легочной артерии вышеуказанные признаки могут быть слабо выражены или отсутствовать совсем. Лишь спустя несколько дней может появиться небольшая температура, кровохарканье и боль в области ребер, усиливающаяся при дыхании. Чаще всего такой характер боли свидетельствует об инфаркте небольшого участка легкого. Если же происходит закупорка крупной артерии, то вышеуказанные клинические признаки проявляются в полной мере, вплоть до острой
дыхательной недостаточности, коллапса и гибели больного в течение нескольких минут или часов.
Диагностика тромбоэмболии легочной артерии
При подозрении на тромбоэмболию легочной артерии следует в кратчайшие сроки определить уровень D-димеров в крови. Данное исследование не подтверждает диагноз окончательно, поскольку его значения могут быть завышены и при других патологических состояниях, однако с его помощью можно исключить тромбоэмболию, когда значения D-димеров остаются в пределах нормы.
На электрокардиограмме могут отмечаться лишь косвенные признаки тромбоэмболии легочной артерии, в частности, признаки перегрузки правых отделов сердца (
заостренный зубец P, отклонение электрической оси вправо, новая блокада правой ножки пучка Гиса, отрицательные зубцы Т в V1 - V4 и др.).
На рентгенографии определяется увеличение правых отделов сердца, локальное снижение интенсивности легочного рисунка, дисковидные ателектазы. При развитии инфаркта легкого, отмечаются четкие, отграниченные конусовидные тени, а также закрытие реберно-диафрагмальных синусов плевральным выпотом с соответствующей стороны.
Эхокардиография может указать на признаки повышения давления в легочной артерии и правых отделах сердца.
Спиральная компьютерная томография позволяет непосредственное обнаружение тромбов в вервях легочной артерии.
Вентиляционно-перфузионная сцинтиграфия выявляет участки легких, которые вентилируются, однако не кровоснабжаются, что свидетельствует о вероятной тромбоэмболии легочной артерии.
Необходимый специалист при тромбоэмболии легочной артерии
Заподозрить тромбоэмболию легочной артерии по клиническим признакам достаточно проблематично, поскольку большое число заболеваний обладает схожей клинической картиной. Тем не менее, заподозрить ее должен быть в состоянии врач любой специальности. Более точной диагностикой и лечением занимается врач-кардиолог.
Методы лечения тромбоэмболии легочной артерии
Медикаментозные методы лечения подразумевают поддержание гемодинамики (
сосудосуживающие препараты) и дыхания (
кислородотерапия, искусственная вентиляция легких). Предотвращение роста тромба и новых тромбоэмболий проводится путем назначения антикоагулянтов (
гепарин, фраксипарин и др.). Удаление тромба производится путем использования тромболитических препаратов (
урокиназа, стрептокиназа и др.). У пациентов с высоким риском повторных тромбоэмболий легочной артерии показана установка кава-фильтров в просвете нижней полой вены.
Боли за грудиной при пневмотораксе
![]()
Пневмоторакс является патологическим состоянием, при котором возникает сообщение между атмосферным воздухом и плевральной полостью, в результате чего происходит спадение легкого на стороне поражения.
Причины пневмоторакса
Пневмоторакс может быть первичным и вторичным. Первичный пневмоторакс развивается на условно здоровом легком, чаще всего по причине разрыва буллы (
небольшой пузырь на поверхности легкого). Вторичный пневмоторакс развивается на фоне заболеваний легких и плевры. В число вторичных пневмотораксов входит также и ятрогенный (
вызванный врачебным вмешательством) пневмоторакс. Его причиной чаще всего является прокол легкого при пункции плевральной полости.
Симптомы пневмоторакса
Главным симптомом является одышка, выраженность которой зависит от количества воздуха в плевральной полости. Иногда отмечаются боли, локализация которых зависит от места разрыва буллы или раздражения плевры.
Диагностика пневмоторакса
Диагностика во многом основывается на физикальном обследовании пациента. При пневмотораксе перкуторно отмечается тимпанический звук, а при аускультации – отсутствие дыхания над спавшимся легким.
Рентгенологическая диагностика также не вызывает затруднений. В прикорневой зоне находится спавшееся легкое, а на периферии – области лишенные сосудистого рисунка.
Необходимый специалист при пневмотораксе
Диагноз пневмоторакса может установить врач любой специальности, поскольку он относится к числу неотложных состояний. Лечением данной патологии занимается врач-пульмонолог.
Методы лечения пневмоторакса
Небольшие пневмотораксы разрешаются самостоятельно без медикаментозного вмешательства в течение нескольких дней. Средние и выраженные пневмотораксы нуждаются в пункции грудной клетки и выпускании лишнего воздуха наружу. Помимо этого, рекомендуется выяснить причину, приведшую к данному состоянию, и заняться ее устранением.
В некоторых случаях приходится прибегать к оперативному вмешательству, целью которого является сшивание плевры и устранение буллы, разрыв которой чаще всего приводит к пневмотораксу.
Боли за грудиной при медиастинальной эмфиземе
![]()
Медиастинальная эмфизема или пневмомедиастинум является патологическим состоянием, при котором в средостении скапливается воздух, смещая находящиеся в нем органы и структуры и препятствуя их нормальному функционированию.
Причины медиастинальной эмфиземе
Попадание воздуха в средостение происходит, как правило, при нарушении целостности бронхов или трахеи во время травмы, после оперативных вмешательств по пересадке легких или во время
бронхоскопии с биопсией бронхиальной стенки. Реже доступ воздуха в средостение осуществляется через дефект пищевода вследствие разрыва дивертикула, неосторожной эндоскопии или бужирования.
Симптомы медиастинальной эмфиземы
Наиболее распространенными симптомами являются давящая загрудинная боль, одышка, посинение кожных покровов и слизистых оболочек, переполнение шейных вен. При распространении воздуха в подкожную клетчатку (
подкожная эмфизема) пальпаторно ощущается крепитация. Наиболее часто подкожная эмфизема распространяется на грудную клетку и шею. Границы относительной тупости сердца становятся трудноразличимыми.
Диагностика медиастинальной эмфиземы
Диагностика пневмомедиастинума основывается на данных физикального обследования и рентгенологических методов. Наиболее простым и доступным методом является простая рентгенография в прямой и боковой проекции. Данный метод выявляет расширение границ средостения и компрессию легких. Если медиастинальная эмфизема развилась из-за нарушения целостности бронха, то на рентгенограмме будут присутствовать признаки полного или частичного спадения соответствующего легкого. Аналогичные изменения можно выявить при КТ или МРТ грудной клетки.
Необходимый специалист при медиастинальной эмфиземе
Диагностика и лечение эмфизем средостения с легким и умеренным течением находится в компетенции пульмонолога. При напряженных и клапанных пневмомедиастинумах требуется срочное вмешательство торакального хирурга.
Методы лечения медиастинальной эмфиземы
В связи с тем, что в небольших количествах воздух из средостения самостоятельно рассасывается в течение нескольких дней, специфического лечения не требуется. Тем не менее, пациентам с одышкой рекомендуется кислородная терапия. При прогрессирующих клапанных эмфиземах средостения необходимо оперативное вмешательство, направленное на устранение дефекта, через которое воздух попадает в данную полость. При подготовке к операции и некоторое время спустя назначаются антибиотики широкого спектра действия с целью профилактики медиастинита.
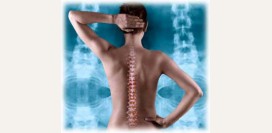
Боли за грудиной при остеохондрозе
![]()
Остеохондроз представляет собой заболевание позвоночного столба, при котором происходит уплощение межпозвоночных дисков и вызванное этим сдавление корешков спинномозговых нервов. В начальных стадиях поражается преимущественно шейный и поясничный отдел
позвоночника, после чего заболевание распространяется и на грудной его отдел.
Причины остеохондроза
Остеохондроз проявляется рано или поздно у всех людей, поскольку его развитие непосредственно связано с процессами старения всего организма. Уменьшение эластичности межпозвоночных дисков развивается по многим причинам. В частности, речь идет о постепенном замедлении обмена веществ, нарушении водно-электролитного баланса и уменьшении количества эластических волокон. Таким образом, можно сказать, что остеохондроз является генетически отчасти запрограммированным процессом.
Тем не менее, существуют факторы, которые приводят к более ранней дегенерации межсуставных дисков. В число данных факторов входит род деятельности, связанный с ношением тяжестей, многочасовой вибрацией, нервным и физическим истощением. Снижение амортизационной функции скелета при
плоскостопии, вальгусной или варусной деформации ног, дисплазии тазобедренных суставов и уменьшении физиологических изгибов позвоночника также приводит к большим нагрузкам на межпозвоночные диски, из-за чего последние скорее изнашиваются.
Курение,
алкоголизм,
переохлаждения, частые травмы позвоночника приводят к более раннему развитию остеохондроза.
Симптомы остеохондроза
Наиболее распространенными жалобами больных остеохондрозом являются боли в проекции позвоночного столба и межреберных нервов, возникающие из-за сдавления корешков спинномозговых нервов. Типичным для данных болей является их острый, колющий характер, а также усиление во время движений, длительного нахождения в положении сидя и во время дыхания (
при задержке дыхания боли исчезают). Помимо этого может отмечаться усиление кожной чувствительности на участках кожи, соответствующих зонам иннервации сдавленных нервных корешков, а также одностороннее увеличение тонуса межреберных мышц и мышц спины.
Тем не менее, в некоторых случаях боли при остеохондрозе могут имитировать загрудинные боли как при стенокардии настолько натурально, что даже опытные врачи затрудняются в постановке диагноза.
Диагностика остеохондроза
Диагностика остеохондроза включает в себя определение соответствующих клинических признаков и использование разнообразных визуализирующих методов для выявления дефектов позвоночного столба.
Наиболее распространенным и недорогим методом является рентгенография грудного отдела позвоночника в двух проекциях, на которой выявляются косвенные признаки нарушения целостности позвоночных дисков – уменьшение расстояния между телами позвонков. Аналогичный характер болей свойственен сдавлению нервных корешков наростами на телах и дугах позвонков, так называемыми
остеофитами, которые на рентгене представляют собой патологические костные остроконечные или дугообразные разрастания чаще по краям суставных поверхностей.
КТ, являясь рентгенологическим методом, в той или иной мере может выявить форму и структуру самих межпозвоночных дисков, однако самым точным инструментальным методом визуализации межпозвоночных дисков является МРТ. Ее преимущество перед КТ заключается в более четком контрастировании структур, богатых жидкостью. Поскольку межпозвоночные диски более чем на 90% состоят из жидкости, данный метод наиболее качественно и детально выявит любые структурные изменения в них и поможет точно определить тяжесть и распространенность остеохондроза.
Помимо подтверждения самого остеохондроза необходимо также исключить заболевания, которые могли бы проявиться такими же болями в грудной клетке. Основными из них являются заболевания сердечно-сосудистой и дыхательной системы. Таким образом, для дифференциального диагноза может использоваться электрокардиография и эхокардиография. Ультразвуковое исследование плевральных полостей поможет диагностировать сухой плеврит, который может быть причиной болей, аналогичных остеохондрозу.
Необходимый специалист при остеохондрозе
Специалистами, занимающимися диагностикой и лечением остеохондроза, являются невролог и нейрохирург. При их отсутствии можно обратиться к терапевту или семейному доктору.
Методы лечения остеохондроза
Наиболее признанным подходом к лечению остеохондроза грудного отдела позвоночника является комплексный подход с использованием как медикаментозных, так и немедикаментозных методов. Медикаментозное лечение направлено на купирование болевого синдрома путем снижения воспаления спинномозговых корешков. Часто применяются лекарственные средства периферического сосудорасширяющего действия, улучшающие кровоснабжение и обмен веществ ишемизированной зоны позвоночника.
Немедикаментозных методов лечения остеохондроза достаточно много, причем их эффективность не всегда соответствует ожиданиям. Физиотерапевтические методы, такие как массаж, гидротерапия, бальнеотерапия и лечение минеральными водами проводятся с целью улучшения микроциркуляции в области сдавленных нервных корешков и устранения мышечного спазма. Хороший противовоспалительный и регенераторный эффект оказывает
ультравысокочастотная терапия,
магнитотерапия и ультразвук, однако использование данных методов допускается лишь в том случае, если у больного на момент лечения нет злокачественных новообразований. Иными словами, опухолевые процессы являются прямым противопоказанием к использованию вышеуказанных физиотерапевтических методов в связи с высоким риском ускорения их роста.
Боли за грудиной при спазме пищевода
![]()
Спазм пищевода представляет собой временное сужение его просвета из-за стойкого сокращения мышечных волокон, в результате избыточного патологического раздражения нервных рецепторов слизистой пищевода.
Причины спазма пищевода
Первичный спазм пищевода происходит из-за врожденного несовершенного развития нервного аппарата данного органа. Из-за этого последний реагирует чрезмерным сокращением не только на нормальные раздражители (
пищевой комок), но и на сторонние, не связанные с пищеварительным актом стимулы, такие как стрессы, физическая нагрузка, боли при патологии соседних органов и др.
Вторичный спазм пищевода развивается при чрезмерном раздражении здорового, полноценно развитого органа. В частности, причинами вторичного спазма может быть проглатывание сухой, твердой, острой или плохо пережеванной пищи, которая механически ранит слизистую оболочку пищевода. Также травмирование и рефлекторный спазм пищевода может случиться при употреблении крепких алкогольных напитков, кислот или щелочей.
Симптомы спазма пищевода
Любой спазм пищевода проявляется невозможностью проглатывания пищи и болевым синдромом. Если невозможность глотания и обратная регургитация пищи является более или менее постоянным симптомом, то выраженность и характер болевого синдрома могут варьировать. Таким образом, на выраженность болей влияет время, на протяжении которого пищевод спазмируется, протяженность спазмированного участка, а также степень расширения пищевода выше спазма. Иными словами, кратковременный спазм (
10 - 15 секунд) значительно менее болезнен, чем длительный спазм (
несколько часов). Спазм только нижнего сфинктера пищевода менее болезнен, нежели диффузный спазм, когда сокращаются не только места физиологических сужений данного органа, но и весь его мышечный слой. Проглатывание пищи в момент спазма приводит к резкому усилению болей, в то время как постепенное накопление слюны в пищеводе менее болезненно.
Момент наступления спазма больной может отметить с точностью до секунды, в то время как исчезновение спазма происходит постепенно. Локализация болей чаще всего загрудинная. Реже боли могут отдавать в живот, спину, ключицы и даже нижнюю челюсть. Высокая интенсивность, загрудинная локализация и высокая длительность болей (
при многочасовых спазмах) требует проведения дифференциального диагноза с сердечной патологией.
Диагностика спазма пищевода
Диагностика спазма пищевода осуществляется на основе клинической картины, рентгенографии с контрастным веществом в нескольких проекциях, а также при помощи
ФЭГДС.
Клиническая диагностика упомянута выше. При подозрении на спазм пищевода выполняют рентгеноскопию с наполнением данного органа сульфатом бария, который является непроницаемым для рентгеновских лучей и выявляет любые дефекты наполнения. При спазме пищевода будет наблюдаться полная или частичная его непроходимость, а также расширение границ пищевода выше спазма.
Более детальным и достоверным исследованием, направленным на выяснение причины спазма, является ФЭГДС. Преимуществом данного метода является возможность визуализировать слизистую пищевода такой, какая она есть на самом деле. Нарушение ее целостности может иметь некоторые особенности (
ожоговое, травматическое, бактериальное, грибковое и др.), что является полезным для определения причины спазма и назначения правильного лечения.
Необходимый специалист при спазме пищевода
При спазме пищевода следует обратиться к гастроэнтерологу.
Методы лечения спазма пищевода
Методы лечения спазма пищевода должны исходить из вызвавшей его причины. При первичных и функциональных неврогенных спазмах рекомендуется применение спазмолитических средств (
папаверин) на фоне приема
успокоительных препаратов (
экстракт валерьяны, экстракт пассифлоры, феназепам и др.). При вторичных посттравматических спазмах на фоне
эзофагитов к спазмолитической терапии рекомендуется добавить антибиотики, нестероидные противовоспалительные средства и местные
обезболивающие препараты. При спазме на фоне желудочно-пищеводного рефлюкса следует понизить кислотность
желудка при помощи препаратов группы ингибиторов протоновой помпы (
пантопразол, лансопразол, рабепразол и др.) и H2-блокаторов гистаминовых рецепторов (
фамотидин, ранитидин и др.).
Хорошим антиспастическим эффектом обладают нитраты (
нитроглицерин, изосорбида мононитрат) и блокаторы кальциевых каналов (
нифедипин, дилтиазем и др.), однако при их использовании обязательно следует учитывать их выраженное влияние на сердечно-сосудистую систему.
Бужирование пищевода (
восстановление его проходимости путем проталкивания жесткого зонда) при его спазме проводится редко, в связи с высокой эффективностью медикаментозного лечения, однако в наиболее тяжелых случаях данный метод может принести некоторую пользу.
Боли за грудиной при ахалазии кардии
![]()
Ахалазия кардии представляет собой хроническое
заболевание пищевода, при котором происходит патологическое смыкание нижнего пищеводного сфинктера в момент проглатывания пищи. В результате, пища застаивается в самом пищеводе, приводя к его расширению.
Причины ахалазии кардии
Причины данной патологии до конца не изучены, однако предполагается, что ее развитие связано с дефектами иннервации нижнего пищеводного сфинктера.
Симптомы ахалазии кардии
Наиболее распространенным симптомом при ахалазии пищевода является дисфагия или нарушение проглатывания пищи. Данный симптом проявляется чувством кома в загрудинном пространстве, которое возникает через несколько секунд после проглатывания пищи. Боли при ахалазии кардии встречаются достаточно часто, причем их усиление наблюдается после еды, что связывается с расширением вышерасположенного отдела пищевода. Для данных болей типичной является загрудинная локализация. Реже такие боли могут иррадиировать (
отдавать) в спину, шею и нижнюю челюсть. Из-за болей пациенты часто уменьшают потребление пищи, вследствие чего стремительно худеют.
Регургитация или обратный заброс пищи в ротовую полость является классическим симптомом ахалазии кардии. Ее усиление отмечается при наклоне больного и в положении лежа. Важно отметить, что регургитация является непроизвольной и не сопровождается тошнотой. Часто регургитации сопутствует осиплость голоса.
В четвертой, терминальной стадии заболевания боль может усиливаться за счет развития застойного воспаления пищевода. Содержимое пищевода при этом приобретает гнилостный запах.
Диагностика ахалазии кардии
Наиболее распространенным методом диагностики данного заболевания является рентгеноскопия пищевода с контрастным веществом. При этом выявляется нарушение проходимости пищевода на уровне кардии различной степени выраженности.
При ФЭГДС обращает на себя внимание момент сложного прохождения через нижний пищеводный сфинктер. При более выраженных стадиях болезни отмечается не только место сужения, но и расположенное выше расширение пищевода.
Золотым стандартом диагностики данной патологии является манометрия пищевода, суть которой заключается в измерении давления в различных отделах пищевода в различные фазы глотания. При ахалазии кардии отмечается резкое увеличение давления в области нижнего пищеводного сфинктера.
Необходимый специалист при ахалазии кардии
Диагностика и лечение данного заболевания находится в компетенции гастроэнтеролога.
Методы лечения ахалазии кардии
Медикаментозные методы лечения данной патологии характеризуются лишь относительной эффективностью. Из группы спазмолитиков наиболее выраженным действием на мускулатуру пищевода обладает папаверин. Сравнительно хорошим эффектом обладают нитропрепараты, однако их применение ограничивается в связи с выраженным влиянием на сердечно-сосудистую систему. Бужирование пищевода производит кратковременный эффект, поэтому применяется редко.
Радикальным хирургическим методом лечения на сегодняшний день является имплантация стента, снабженного клапанным механизмом, в области нижнего пищеводного сфинктера. Также разработана методика эндоскопического частичного рассечения мышечных волокон нижнего пищеводного сфинктера, демонстрирующая превосходные результаты.
Боли за грудиной при диафрагмальной грыже
![]()
Диафрагмальная грыжа является патологическим состоянием, при котором происходит выпячивание органов брюшной полости в грудную полость через дефект диафрагмы. Диафрагмальные грыжи подразделяются на истинные и ложные. Истинные грыжи развиваются в слабых местах диафрагмы и имеют грыжевой мешок. Ложные грыжи развиваются при расширении физиологических отверстий диафрагмы и не имеют грыжевого мешка.
Причины диафрагмальной грыжи
Истинная диафрагмальная грыжа развивается длительное время в ослабленном участке диафрагмы. Факторами, приводящими к выпячиванию органов брюшной полости в грудную полость, являются все причины, приводящие к повышению внутрибрюшного давления. В частности, к ним относится затяжной
кашель, рвота,
запоры,
асцит, крупная опухоль, частые травмы (
борцы, боксеры) и многое другое. Одномоментное образование и ущемление грыжи может произойти при резком и значительном повышении внутрибрюшного давления во время падения, ДТП (
например, наезд на пешехода), сдавливания туловища завалами при землетрясениях и т. п.
Формированию ложной грыжи (
грыжи пищевода) способствует постепенное расширение пищеводного отверстия диафрагмы. В результате в грыжевых воротах может находиться пищевод, часть желудка, а также петля тонкого кишечника или сальник.
Симптомы диафрагмальной грыжи
Основными симптомами диафрагмальной грыжи являются боли за грудиной, изжога и одышка.
Интенсивность болевого синдрома может варьировать в зависимости от того, происходит ли ущемление органов в грыжевых воротах или нет. При ущемлении грыжи происходит острое нарушение кровоснабжения находящегося в грыжевом мешке органа. При неразрешении данного осложнения в ближайшие полтора - два часа происходит некроз органа и развитие перитонита.
Изжога развивается из-за расширения нижнего пищеводного сфинктера и попадания желудочного сока в пищевод. Одышка является следствием компрессии легочной ткани со стороны органов брюшной полости, находящихся в грыже.
Диагностика диафрагмальной грыжи
Диагностика диафрагмальной грыжи осуществляется на основании обзорной рентгенографии грудной и брюшной полости с использованием контрастного вещества. При данном исследовании четко визуализируются структуры желудочно-кишечного тракта, проникающие в грудную полость через дефект диафрагмы.
Необходимый специалист при диафрагмальной грыже
При подозрении на диафрагмальную грыжу следует обратиться к гастрологу, а при необходимости и к хирургу.
Методы лечения диафрагмальной грыжи
Диафрагмальные грыжи лечатся преимущественно симптоматически путем назначения препаратов, снижающих кислотность желудочного сока и, как следствие, уменьшающих болевые ощущения и
изжогу. Тяжелые формы заболевания лечатся хирургически в плановом порядке путем ушивания грыжевых ворот и возвращения органов обратно в брюшную полость. Ущемленные диафрагмальные грыжи лечатся комбинированно – медикаментозно (
спазмолитики) и хирургически в экстренном порядке.
Боли за грудиной при опухолях средостения
![]()
Опухолью называется область неконтролируемого роста клеток определенного типа. В зависимости от степени дифференцированности клеток различают доброкачественные и злокачественные опухоли. Доброкачественные опухоли обладают высокой степенью дифференциации и, как следствие, медленным ростом и невозможностью метастазирования (
поскольку они не распадаются). Злокачественные опухоли состоят из низкодифференцированных (
атипичных) клеток, поэтому растут и распадаются быстрее. В результате их распада происходит распространение метастазов опухоли по всему организму.
Причины опухолей средостения
Причин злокачественного перерождения тех или иных тканей организма множество. Наиболее доказанным считается онкогенное влияние ионизирующей радиации, некоторых химических веществ.
Стрессы, курение, злоупотребление алкогольными напитками также увеличивают вероятность
рака. При некоторых видах опухолей существует достаточно высокая вероятность наследственной предрасположенности.
Симптомы опухолей средостения
Клиническая картина опухолей средостения во многом зависит от их природы и степени развития. Доброкачественные опухоли средостения встречаются редко и представляют собой в основном
липомы с крайне медленным ростом. Больные с такими опухолями могут списывать ее симптомы (
одышка и тупая боль за грудиной) на признаки старения и не обращать на них внимания на протяжении многих лет.
Со злокачественными опухолями дело обстоит иначе. Даже при небольших размерах они могут метастазировать в региональные лимфоузлы средостения и приводить к их стремительному росту. Таким образом, от момента возникновения опухоли до появления ее признаков проходит гораздо меньше времени. Кроме того, если данная опухоль соседствует с плеврой, то велика вероятность накопления транссудата в плевральной полости, который сдавливал бы легкое, смещал средостение в сторону и нарушал работу сердца. Нагноение транссудата приводит к развитию клинической картины эмпиемы плевры.
Диагностика опухолей средостения
При обычной рентгенограмме можно определить расширение средостения. Наиболее точный диагноз устанавливается на основании КТ, МРТ и медиастиноскопии с биопсией ткани опухоли и увеличенных лимфатических узлов.
Необходимый специалист при опухолях средостения
При подозрении на опухоль средостения следует обратиться к онкологу, а при необходимости и к торакальному хирургу.
Лечение опухолей средостения
Лечение доброкачественных опухолей является только хирургическим и выполняется в плановом порядке с надлежащей подготовкой к нему пациента.
Лечение злокачественных опухолей зависит от их гистологического типа и стадии. По гистологическому типу можно судить о том, насколько эффективным ожидается лечение химиопрепаратами и облучением (
разные опухоли по-разному реагируют на различные химиопрепараты), а также насколько интенсивным оно должно быть. От стадии опухоли зависит то, какое количество жизнеспособных тканей необходимо удалить вместе с опухолью для полного ее излечения. При последних стадиях злокачественного процесса лечение, к сожалению, лишь паллиативное и заключается преимущественно в обезболивании наркотическими анальгетиками и уходом за пациентом.
Боли за грудиной при инфаркте легкого
![]()
Инфаркт легкого представляет собой патологическое состояние, как правило, развивающееся вследствие тромбоэмболии одной из ветвей легочной артерии. В результате, происходит острое нарушение кровоснабжения участка легочной ткани, поскольку объем кровотока по бронхиальным артериям недостаточен для поддержания ее жизнеспособности. Воспалительная реакция в очаге инфаркта легкого приводит к скоплению в его альвеолах крови. Часто происходит наслоение бактериальной или грибковой инфекции, приводящее к тяжелым
пневмониям.
Причины инфаркта легкого
Причиной инфаркта легкого является тромбоэмболия легочной артерии (
ТЭЛА). ТЭЛА, в свою очередь, развивается при заносе эмбола из системного кровотока (
чаще глубокие вены ног) или формирования тромба непосредственно в просвете одной из ветвей легочной артерии.
Симптомы инфаркта легкого
К наиболее распространенным симптомам инфаркта легких относят остро возникшую одышку, ассоциированную с кровохарканьем и загрудинными болями. При большой площади инфаркта отмечаются признаки острого
легочного сердца (
увеличение сердечного толчка в области мечевидного отростка). Перегрузка правого предсердия может спровоцировать нарушения сердечного ритма, которые, в свою очередь, приводят к повышению или снижению артериального давления. В редких случаях могут отмечаться выраженные вегетативные реакции, такие как тошнота, рвота,
диарея,
боли в животе по типу
кишечных колик и др.
Диагностика инфаркта легкого
Поскольку практически всегда инфаркт легкого развивается на фоне ТЭЛА, следует при первых же ее признаках исследовать уровень D-димеров в периферической крови, который должен быть повышен. В качестве дифференциального диагноза с инфарктом миокарда в числе срочных исследований исследуют тропонины (
при ТЭЛА отрицательны).
Наиболее четко визуализировать инфаркт легкого можно при помощи компьютерной томографии с ангиографией легочной артерии, выполненной параллельно с радиоизотопным сканированием легких. КТ с ангиографией выявляет участки отсутствия кровоснабжения легких, а радиоизотопное сканирование выявляет участки легких, в которые не проникает воздух. В результате, если в одном и том же участке легких выявляется отсутствие кровоснабжения и аэрации, это свидетельствует в пользу инфаркта легкого. Однако, к сожалению, данное исследование можно провести лишь в крупных кардиологических центрах, и стоит оно значительно больше, чем месячный оклад среднестатистического больного.
Помимо вышеперечисленных исследований можно произвести обычную рентгенографию, которая в совокупности со специфической клинической картиной может натолкнуть врача на верный диагноз. Также в пользу инфаркта легкого будет свидетельствовать резко возникшая перегрузка правых отделов сердца на ЭКГ и увеличение давления в легочной артерии и правом желудочке на ЭхоКГ.
Необходимый специалист при инфаркте легкого
Пациенты с подозрением на ТЭЛА и инфаркт легкого госпитализируются в отделение интенсивной терапии.
Методы лечения инфаркта легкого
При инфаркте легкого назначаются наркотические обезболивающие средства, прямые и непрямые антикоагулянты (
при отсутствии кровохарканья), метилксантины (
эуфиллин), коллоидные растворы и др. Присоединение пневмонии предполагает назначение антибиотиков или противогрибковых препаратов.
Боли за грудиной при прободной язве желудка или двенадцатиперстной кишки
![]()
Прободной язвой называется нарушение целостности всех слоев полостного органа (
желудка или кишечника), в результате которого происходит выход их содержимого в брюшную полость.
Причины возникновения прободной язвы
Наиболее распространенной причиной развития язв является прямое разрушающее действие бактерии под названием Helicobacter Pylori. Также прямым и опосредованным цитотоксическим эффектом на слизистую оболочку полостных органов обладает этиловый спирт, никотин и неселективные противовоспалительные лекарства, детергенты и др.
Симптомы прободной язвы
Прободная язва обычно развивается в течение как минимум нескольких недель. В этот период больной испытывает волнообразно возникающие тупые, ноющие боли. Помимо этого, могут возникать периодические
желудочно-кишечные кровотечения, проявляющиеся рвотой кровью цвета «кофейной гущи» и черным жидким стулом. Отмечается резкая слабость, головокружение, сердцебиение, бледность кожных покровов, холодный и липкий пот, потеря сознания. Момент прободения язвы характеризуется острой кинжальной болью в эпигастральной области (
в проекции желудка, под ложечкой) или несколько правее в случае прободения язвы двенадцатиперстной кишки. Через несколько часов данная боль смещается в правую паховую область живота, имитируя острый
аппендицит. Также обращают на себя внимание признаки поражения брюшины, такие как локальное, а затем и разлитое уплотнение мышц живота (
«доскообразный живот»), поднятие температуры тела до 38 и более градусов, диспептические явления (
тошнота, рвота, диарея и др.), положительные симптомы раздражения брюшины (
Блюмберга, Воскресенского и др.).
Вышеописанная клиническая картина прободной язвы считается классической, однако в некоторых случаях боли в эпигастрии могут иррадиировать (
отдавать) в грудную клетку, имитируя приступ стенокардии или даже острый инфаркт миокарда.
Диагностика прободной язвы
Наиболее точным инструментальным методом диагностики прободной язвы является ФЭГДС, при которой определяется дефект стенки желудка или двенадцатиперстной кишки. В отсутствии данного метода можно использовать рентгеноскопию с контрастным веществом. Однако в данном случае стоит сделать поправку, что при подозрении на перфорацию полостного органа в качестве контраста запрещено использовать сульфат бария, поскольку при контакте с брюшиной он вызывает специфический бариевый перитонит. Вместо него используются водорастворимые контрастные вещества, например, урографин. УЗИ чаще используется для дифференциальной диагностики с другими заболеваниями. Общий анализ крови выявит лейкоцитоз и сдвиг лейкоцитарной формулы влево (
увеличение количества молодых форм нейтрофилов). Для исключения сердечной патологии необходимо сделать кардиограмму и измерить уровень тропонинов в крови.
Необходимый специалист при прободной язве
При подозрении на данное заболевание рекомендуется консультация хирурга.
Методы лечения прободной язвы
Лечение прободной язвы исключительно хирургическое. Его объем зависит преимущественно от величины язвы и ее локализации. В наиболее простых случаях выполняется ушивание язвы, а в более тяжелых – удаление части желудка или кишечника с соответствующей пластикой (
восстановление целостности и проходимости пищеварительного тракта).
Боли за грудиной при остром холецистите
![]()
Острый холецистит представляет собой бурно протекающее воспаление желчного пузыря.
Причины острого холецистита
Чаше всего развитие данного заболевания связано с острым нарушением оттока желчи вследствие закупорки протока желчного пузыря камнями. Реже закупорка может произойти гельминтами. Развитие бескаменного холецистита происходит в основном как осложнение сопутствующих патологических состояний (
сепсис, массивные ожоги, полиорганная недостаточность и др.).
Симптомы острого холецистита
Классическими симптомами острого холецистита являются боли в правом подреберье, повышение температуры тела до 37,5 - 38,5 градусов, тошнота,
горечь во рту и реже желтуха. В некоторых случаях боли при остром холецистите могут отдавать в правую подключичную область, правую лопатку, позвоночник и даже в правую половину шеи.
Диагностика острого холецистита
Диагностика острого холецистита основывается преимущественно на клинических данных, а также на изменении формы и структуры желчного пузыря на УЗИ. Общий анализ крови выявляет неспецифические признаки воспаления (
лейкоцитоз и сдвиг лейкоцитарной формулы влево). К более дорогостоящим методам, таким как КТ, прибегают редко.
Необходимый специалист при остром холецистите
При подозрении на острый холецистит необходима консультация хирурга.
Методы лечения острого холецистита
Если позволяет состояние больного, то прибегают к усиленному спазмолитическому лечению (
папаверин, дротаверин, мебеверин и др.). Температуру снижают при помощи нестероидных противовоспалительных средств (
парацетамол, ибупрофен) или литических смесей (
анальгин + димедрол).
Если состояние больного тяжелое и подозревается развитие осложнений (
подпеченочный абсцесс, гангрена желчного пузыря, перитонит, сепсис и др.) то осуществляется экстренное хирургическое удаление желчного пузыря и иссечение расположенных вокруг нежизнеспособных тканей. На сегодняшний день большинство операций выполняются лапароскопически через несколько небольших надрезов в брюшной стенке.
Боли за грудиной при панкреонекрозе
![]()
Панкреонекрозом называется выраженное воспаление с элементами некротического отторжения части или всей поджелудочной железы из-за ее внутрипротоковой активации ее собственных
ферментов.
Причины панкреонекроза
Наиболее часто панкреонекроз развивается вследствие злоупотребления алкогольными напитками. Также исследования последних лет в данной области указывают на выраженное прямое токсическое действие никотина на ткани поджелудочной железы.
Существует также ряд факторов, которые увеличивают вероятность развития панкреонекроза. К числу таковых относится оперативное вмешательство в области общего желчного протока и сфинктера Одди, опухоль головки поджелудочной железы, камни в желчном пузыре и глистная инвазия.
Симптомы панкреонекроза
Среди симптомов доминирует боль в эпигастральной области, интенсивность которой обычно соответствует выраженности воспаления. Тем не менее, не редки случаи панкреонекроза с болями небольшой и умеренной интенсивности, иррадиирующими (
отдающими) за грудину. Вторым важным симптомом является шоковое состояние (
резкое снижение артериального давления), которое проявляется резкой слабостью, головокружением, потерей сознания, сердцебиением, бледными кожными покровами, холодным липким потом и др. Может отмечаться умеренное повышение температуры тела.
Диагностика панкреонекроза
Диагностика основывается на характерной клинической картине, лабораторных данных и УЗИ. Характерным признаком панкреонекроза является чрезмерно высокий уровень ее ферментов в крови и моче. На УЗИ поджелудочная железа негомогенна (
неоднородна), увеличена. В забрюшинном пространстве и в малом сальнике отмечаются скопления жидкости. В крайних случаях выполняется диагностическая
лапароскопия.
Необходимый специалист при панкреонекрозе
При подозрении на панкреонекроз необходимо в срочном порядке обратиться к хирургу.
Методы лечения панкреонекроза
Консервативные методы лечения заключаются в применении спазмолитических (
папаверин, дротаверин, мебеверин и др.) и антиферментных (
гордокс) препаратов. Некоторые представители нестероидных противовоспалительных препаратов (
нимесулид, мелоксикам и др.) успешно останавливают прогрессию панкреонекроза.
Хирургическое лечение данного заболевания чрезвычайно сложно и зачастую неэффективно. Основная проблема данных операций заключается в том, что иссечение отмерших тканей скальпелем приводит к прогрессии некроза. Оптимальным способом лечения является бережное удаление отторгшихся частей железы зажимами или тупыми концами скальпелей, совмещенное с приемом лекарств, перечисленных выше.
Боли за грудиной при холедохолитиазе
![]()
Холедохолитиазом называется патологическое состояние, при котором происходит закупорка общего желчного протока камнями желчного пузыря. В результате, происходит нарушение оттока желчи, ее застой в печени и повышение уровня билирубина в крови. От высокого уровня билирубина в первую очередь страдают нейроны головного мозга. К тому же застой желчи вызывает расширение общего желчного протока и внутрипеченочных желчных путей, что в совокупности с присоединением бактериальной инфекции вызывает выраженный токсико-инфекционный синдром.
Причины холедохолитиаза
Холедохолитиаз развивается из-за закупорки общего желчного протока камнями, образовавшимися в желчном пузыре. Формирование камней в желчном пузыре происходит при нарушении обмена желчных кислот в организме, развивающееся у людей, в избытке употребляющих продукты, богатые насыщенными желчными кислотами (
маргарин и кондитерские изделия на его основе).
Симптомы холедохолитиаза
Классическими симптомами холедохолитиаза являются боли в правом подреберье, интенсивная желтуха и высокая температура тела (
более 38 градусов). Стул, как правило, ахоличен (
не имеет характерной коричневой окраски). Развитие перитонита может сопровождаться присоединением диареи. У некоторых больных происходит иррадиация (
отдача) болей из правого подреберья в грудную клетку, правое плечо, ключицу, лопатку и позвоночник.
Диагностика холедохолитиаза
Диагностика данного заболевания основывается на характерных клинических проявлениях и УЗИ. На УЗИ определяются камни, застрявшие в общем желчном протоке, а также его расширение выше места закупорки. При возникновении сомнений в диагнозе как крайняя мера выполняется диагностическая лапароскопия.
Необходимый специалист при холедохолитиазе
При появлении вышеперечисленных симптомов следует незамедлительно обратиться к хирургу.
Методы лечения холедохолитиаза
Если подтверждается диагноз холедохолитиаза, то чаще всего осуществляется оперативное удаление камней из общего желчного протока с восстановлением его целостности. Обычно такая операция производится через открытый лапаротомический доступ.
В редких случаях может произойти самостоятельное выделение камня в просвет двенадцатиперстной кишки при использовании спазмолитических лекарственных средств. Однако данная выжидательная тактика опасна в связи с высоким риском развития осложнений, таких как желчный перитонит, печеночная
энцефалопатия и др.
Боли за грудиной при перитоните
![]()
Перитонит является патологическим состоянием, при котором происходит воспаление брюшины, выстилающей стенки и окружающей большинство органов брюшной полости.
Причины перитонита
Подавляющее число перитонитов развивается из-за попадания и размножения бактерий на поверхности брюшины. Бактерии могут попасть в брюшную полость при ранениях, в ходе оперативных вмешательств, а также проникать через кишечную стенку при асците или острой
кишечной непроходимости.
Кроме того, воспаление брюшины может развиться и без присутствия патогенных микроорганизмов, в частности, при ее раздражении химическими веществами, содержащимися в желчи, моче, желудочном соке и даже крови.
Симптомы перитонита
Перитонит проявляется резкими болями в пораженной области брюшины при локализованном перитоните и диффузными болями при распространенном перитоните.
Болям сопутствует высокая температура тела (
38 - 40 градусов), однако у ослабленных, пожилых и иммунокомпромисных пациентов может отмечаться только субфебрилитет (
температура тела менее 38 градусов).
На ощупь живот становится твердым, доскообразной плотности. Присутствуют различные симптомы раздражения брюшины (
Щеткина-Блюмберга, Воскресенского, Менделя и др.). В большинстве случаев отмечается рвота, не приносящая больному облегчения. Реже одним из первых признаков данного патологического состояния является диарея.
В некоторых случаях интенсивность болевого синдрома может быть велика насколько, что вызывает иррадиацию (
отдачу) болей в загрудинное пространство, шею, пах и т. д.
Диагностика перитонита
Диагностика данного заболевания основывается на клинической картине, лабораторных данных и параклинических методах, определяющих причину перитонита. Наиболее информативным анализом позволяющим оценить выраженность и степень прогрессии перитонита является общий анализ крови, выявляющий лейкоцитоз с резким сдвигом лейкоцитарной формулы влево и увеличением
СОЭ (скорость оседания эритроцитов). Среди визуализирующих методов применяется панорамная и контрастная рентгенография брюшной полости (
для диагностики острой кишечной непроходимости), УЗИ (
для диагностики панкреонекроза), КТ (
для выявления осумкованных перитонеальных абсцессов), ФЭГДС (
для диагностики прободной язвы желудка и двенадцатиперстной кишки) и др.
В случае локализованного, осумкованного перитонита, при котором клинические проявления размыты, помимо вышеперечисленных методов могут прибегнуть к диагностической лапароскопии.
Необходимый специалист при перитоните
Подозрение на перитонит является прямым показанием к госпитализации в хирургический стационар для выполнения срочного оперативного вмешательства.
Методы лечения перитонита
Лечение данной патологии исключительно хирургическое и состоит во вскрытии брюшной полости, устранении причины перитонита, обработке брюшины антисептическими растворами и ушивании раны. Еще на протяжении недели брюшная полость промывается растворами антисептиков, подаваемых через дренажи, оставленные в нескольких местах передней брюшной стенки, после чего они поочередно удаляются и брюшная полость зашивается полностью.
![]()
Какова причина болей в груди у ребенка?
![]()
Причиной болей в груди у ребенка могут быть заболевания сердца, дыхательной, нервной или других систем.
Боль в груди у ребенка может быть обусловлена: - Клапанными пороками сердца. Суть данной патологии заключается в нарушении структуры клапанов, разграничивающих камеры сердца и необходимых для выполнения им своей насосной функции. Обычно врожденные клапанные пороки выявляются еще при рождении, так как имеют характерные клинические проявления (изменение цвета кожных покровов, недостаток воздуха, нарушение сознания и др.). Однако в некоторых случаях пороки могут быть менее выраженными, вследствие чего проявятся только по мере взросления ребенка, когда он начнет заниматься более интенсивной физической активностью (бегать, прыгать). Выявить клапанный порок сердца можно с помощью простого ультразвукового исследования (эхокардиографии). Прогноз зависит от тяжести самого порока, а также от своевременности диагностических и лечебных мероприятий (если диагноз выставлен слишком поздно, когда уже развились признаки сердечной недостаточности, эффективность проводимого лечения будет крайне низкой).
- Поражением позвоночника. Поражение позвоночного столба может привести к ущемлению спинномозговых нервов, которые проходят между позвонками и иннервируют ткани грудной стенки и органов грудной клетки. Это может стать причиной появления острых колющих болей в груди, которые не связаны с физической нагрузкой (последнее более характерно для сердечных болей). Для постановки диагноза может понадобиться компьютерная томография или магнитно-резонансная томография, с помощью которых можно будет определить уровень и объем поражения.
- Травмой. Дети часто получают травмы во время игр, однако не всегда стремятся рассказать об этом родителям, так как часто боятся быть наказанными. Если ребенок вдруг начал жаловаться на боли в груди, следует раздеть его и внимательно осмотреть грудь и спину в поисках синяков, царапин или ссадин. Также стоит спокойно расспросить малыша, не получал ли он травму в последнее время. Если травма имела место, следует как можно скорее обратиться в травмпункт, где врач осмотрит ребенка и при необходимости назначит рентгенологическое исследование. Не рекомендуется в таких случаях заниматься самолечением, так как боль в груди может быть обусловлена переломами ребер или повреждением внутренних органов.
- Плевритом. Плевритом называется воспаление легочной плевры – тонкой двухслойной оболочки, окружающей легкие и обеспечивающей их расправление во время вдоха. Воспаление плевры может произойти при поражении ее инфекционными агентами (например, при распространении бактерий из очага инфекции при пневмонии). Боли при этом будут появляться или усиливаться во время вдоха или выдоха и будут четко локализованы (ребенок сможет указать пальцем, где его болит). Важно отметить, что при обычном воспалении легких (то есть при пневмонии без вовлечения плевры) болей нет, так как болевые рецепторы имеются только в плевральной оболочке легких, но не в самой легочной ткани.
- Поражением трахеи. При вирусных инфекциях (например, при гриппе) вирус разрушает слизистую оболочку верхних дыхательных путей, в результате чего она становится крайне чувствительной к внешним раздражителям. Вот почему во время кашля (который в первые дни заболевания обычно сухой и мучительный) дети могут жаловаться на выраженную жгучую или колющую, стреляющую боль в груди и боль в горле.
- Поражением пищевода. Воспаление слизистой оболочки пищевода может произойти при его химическом поражении (например, если ребенок выпил уксус или другую опасную жидкость). Также причиной болей может быть инородное тело (например, рыбная косточка), проглоченное ребенком и застрявшее в пищеводе. Ребенок при этом будет крайне беспокоен, может кричать и плакать, жаловаться на колющие или жгучие боли в груди, усиливающиеся во время глотания. Иногда может отмечаться рвота недавно съеденной пищей.
Почему болит грудь при вдохе/дыхании?
![]()
Возникающие или усиливающиеся во время дыхания боли в груди могут указывать на наличие серьезных патологий грудной стенки или внутренних органов грудной клетки.
Боль в груди при дыхании может быть вызвана: Плеврит Каждое легкое окружено особой мембраной – легочной плеврой. Плевра состоит из двух листков - висцерального (
прилегает к легочной ткани) и париетального (
прилегает к внутренней поверхности грудной стенки). Между двумя этими листками образуется замкнутое пространство (
плевральная полость), которое в норме содержит небольшое количество жидкости. Во время вдоха в плевральной полости создается отрицательное давление, за счет чего и происходит расправление легких. При этом висцеральный и париетальный листки плевры довольно легко скользят друг относительно друга, что обеспечивается благодаря наличию плевральной жидкости.
При развитии различных заболеваний легких (
при пневмонии, туберкулезе, травме грудной стенки и др.) патологический процесс может переходить на плевру, в результате чего может развиваться ее воспаление (
плеврит). При этом отмечается отечность плевральных листков и скапливание в плевральной полости большого количества воспалительной жидкости (
экссудата). В результате этого во время вдоха листки плевры трутся друг о друга с большей силой, что приводит к раздражению болевых рецепторов (
которыми они богаты) и появлению болей. В покое (
то есть на пике вдоха или выдоха) листки плевры не трутся друг о друга, болевые рецепторы не раздражатся и боль отсутствует.
Травма грудной стенки При травмировании грудной стенки тупым предметом может развиться ушиб мягких тканей или перелом ребер, что будет сопровождаться болевым синдромом во время дыхания. В случае ушиба боль обусловлена воспалением межреберных мышц, сокращение которых обеспечивает вдох и выдох. При развитии воспалительного процесса травмированные мышцы отекают, а чувствительность болевых рецепторов в области поражения значительно возрастает. В результате этого при каждом вдохе (
то есть при каждом очередном сокращении поврежденных мышц) человек будет испытывать сильную колющую боль в месте удара и в непосредственной близости от него.
В случае перелома ребер также развивается воспалительный процесс, который переходит на мягкие ткани и обуславливает возникновение болей во время вдоха. В то же время костные отломки могут травмировать плевральные листки, что также может являться причиной возникновения или усиления болей.
При болях в грудной клетке после травмы рекомендуется посетить травмпункт и пройти рентгенологическое исследование, что позволить исключить наличие переломов ребер и других осложнений.
Межреберная невралгия Данным термином обозначается патологическое состояние, при котором человек испытывает сильнейшие боли в межреберных промежутках, усиливающиеся во время вдоха, при кашле или чихании, а также во время резкого сгибания или поворота туловища. Боль иногда бывает настолько сильной, что нарушает процесс дыхания (
больной не может вдохнуть).
Причиной межреберной невралгии является повреждение спинномозговых нервов грудного отдела позвоночника. Волокна данных нервов проходят в межреберные промежутки и иннервируют ткани данной области. При повреждении (
сдавливании) спинномозговых нервов (
что может наблюдаться при различных заболеваниях позвоночника – при остеохондрозе, сколиозе, травме, чрезмерной физической) в них возникают патологические болевые импульсы, которые передаются в головной мозг и воспринимаются человеком как колющая, ноющая или жгучая боль в зоне иннервации поврежденного нерва (
то есть в межреберных промежутках).
Лечение межреберной невралгии заключается в устранении причины сдавливания спинномозговых нервов (
хирургически или терапевтически), а также в симптоматическом назначении болеутоляющих препаратов, миорелаксантов (
препаратов, расслабляющих мышцы и снижающих выраженность болей) и других лекарственных средств.
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) Данная патология характеризуется нарушением функции нижнего пищеводного сфинктера (
мышцы), в результате чего пища и кислый желудочный сок забрасываются из желудка в пищевод. В нормальных условиях данный сфинктер закрыт (
то есть перекрывает просвет между пищеводом и желудком), а открывается он лишь во время проглатывания пищи, когда к нему подходит проглоченный пищевой комок. При ГЭРБ отмечается нарушение иннервации нижнего пищеводного сфинктера (
он не смыкается полностью или открывается в отсутствии пищевого комка), в результате чего содержимое желудка может проникать в пищевод. Способствовать данному явлению может глубокий вдох, во время которого происходит сокращение диафрагмы (
дыхательной мышцы, отделяющей грудную полость от брюшной полости). При этом давление в желудке повышается (
особенно после приема большого количества пиши) и его содержимое «выталкивается» в пищевод.
При попадании кислого желудочного сока на слизистую оболочку пищевода она воспаляется и повреждается, в результате чего человек испытывает режущую боль или сильное жжение в груди и иногда в горле (
то есть изжогу). Если во время приступа изжоги выпить стакан воды или что-нибудь съесть, кислый желудочный сок на время нейтрализуется и боль стихнет, однако в ответ на принятую пищу желудочные железы выделят еще больше сока, в результате чего через некоторое время изжога возобновится с новой силой.
Симптоматическое лечение заключается в приеме препаратов, угнетающих секрецию или нейтрализующих уже выделенный кислый желудочный сок (
алмагель, ренни и др.).