Содержание статьи:
Бактериофаги часто преподносят как то, что способно решить проблему антибиотикорезистентности. В качестве подтверждения приводят примеры того, как фагопрепараты помогали при инфекциях, вызванных опаснейшими бактериями, устойчивыми к самым современным антибиотикам.
О преимуществах бактериофаготерапии рассказано много – в том числе и на нашем сайте. Громкие похвалы порой создают ощущение панацеи, но на самом деле это, конечно же, не так. Фаги не лишены недостатков – потому и не заменили до сих пор полностью антибиотики.
Сложность №1: подбор подходящих фагов
В целом выделить вирусы против любых бактерий легко: они во внешней среде повсюду. Сложности начинаются, когда среди них нужно отобрать те, что обладают нужными характеристиками:
- являются вирулентными – то есть уничтожают бактерии сразу после инфицирования;
- уничтожают только нужные микроорганизмы и не трогают представителей микрофлоры;
- не содержат генов, которые могут сделать бактерии устойчивыми к антибиотикам или более опасными для человека.
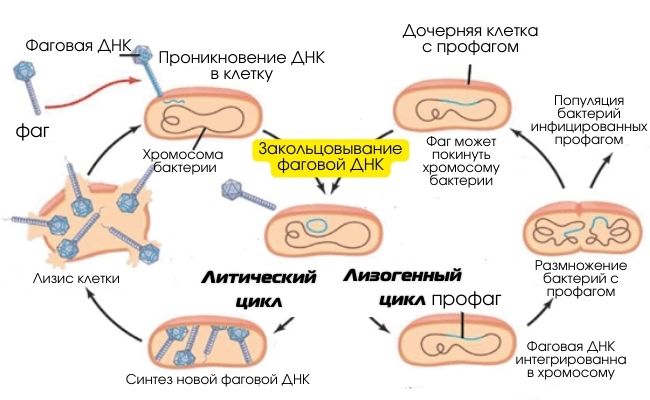
Два основных жизненных цикла фагов: литический и лизогенный. Для терапии хорошо подходят вирулентные фаги, у которых есть только литический цикл. © researchgate.net
Когда нужный фаг найден, встают новые проблемы. Нужно отработать технологию производства препарата, сделать так, чтобы он мог долго храниться и оставаться стабильным. Тут большую роль играют особенности конкретного бактериофага. Для каждого вируса нужно подбирать свои способы стабилизации. На отлаживание всех технологий можно потратить очень много денег и времени. И эти затраты могут не окупиться из-за других ограничений фаготерапии.
Сложность №2: неидеальные убийцы
Фаги часто называют «убийцами бактерий». Но на самом деле природа не создавала их для того, чтобы уничтожать микроорганизмы. Перед фагами стоит совсем другая цель: сохранить и размножить свой генетический материал. Им невыгодно уничтожать всех своих хозяев: ведь тогда и сами они не смогут размножаться. В природе популяции бактерий и фагов существуют в равновесии.
Поэтому от фаготерапии нельзя ожидать того же «тотального геноцида», что и во время лечения антибиотиками. Задача фаготерапии – уничтожить столько вредных микробов, сколько получится, а дальше должна справиться иммунная система пациента. Если она ослаблена, то после фаготерапии состояние может даже ухудшиться.
Сложность №3: к бактериофагам тоже вырабатывается резистентность
Бактерии приспосабливаются не только к антибиотикам, но и к фагам. В их арсенале много средств защиты:
- из-за мутаций могут измениться белки-рецепторы, с помощью которых вирус распознаёт бактериальную клетку и проникает в нее;
- бактерии могут образовать биопленку – массу в виде желе, через которую фагам сложно проникнуть;
- внутри бактериальных клеток действует множество механизмов защиты – что-то вроде иммунной системы у человека;
- некоторые инфицированные бактерии совершают «самоубийство» и тем самым предотвращают заражение соседей.
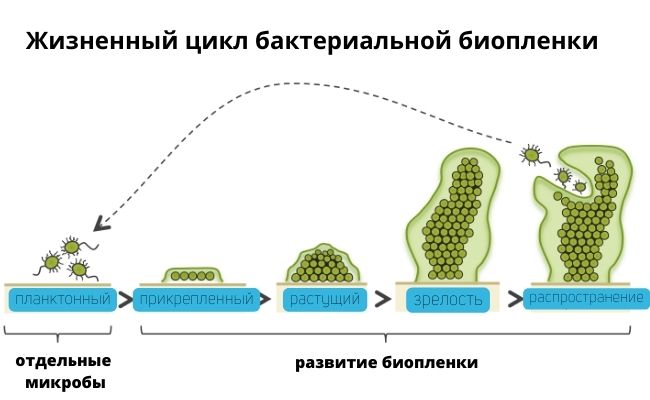
Образование биопленок © bellalindemann.com
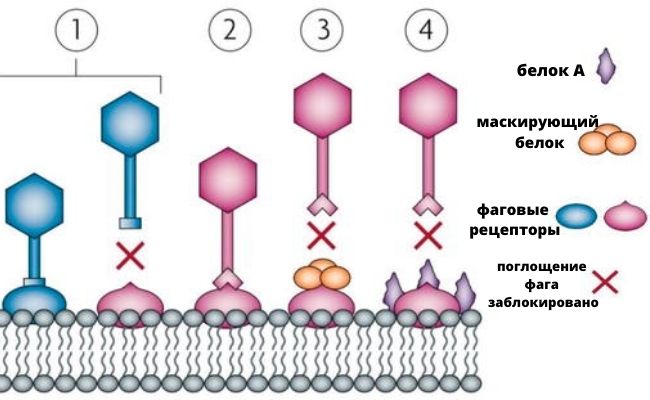
Мутации фаговых рецепторов © intechopen.com
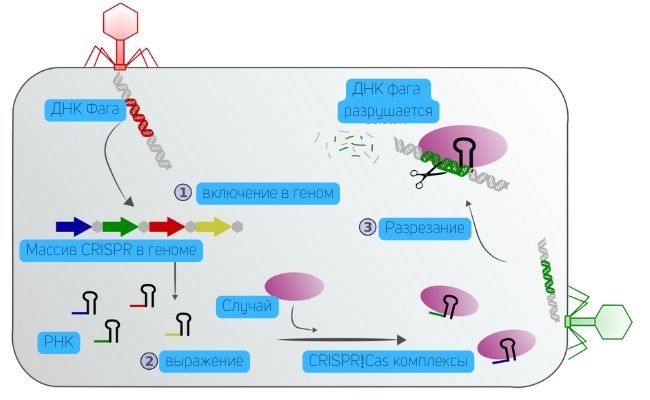
CRISPR-Cas – наиболее знаменитая «иммунная система» бактерий © gesundheitsindustrie-bw.de
Резистентность к фагам не отменяет совсем фаготерапию и не делает ее неэффективной. Ведь фаги тоже эволюционируют, учатся «вскрывать» бактериальную защиту. Но зачастую эта гонка вооружений происходит прямо в процессе лечения. Это одна из причин, почему фаги не могут устроить «тотальный геноцид». Проблему можно решить, если во время лечения постоянно проводить анализы, выводить новые более эффективные фаги, вводить их пациенту. Зачастую такие затраты времени, сил, денег и ресурсов клиник на одного пациента попросту нецелесообразны.
Сложность №4: конфронтация с иммунной системой
Бактериофаги безопасны для человека, но наша иммунная система об этом не знает. Вирусы бактерий воспринимаются как чужеродные антигены и вызывают иммунную реакцию: против них вырабатываются антитела, их поглощают клетки-фагоциты. В итоге эффективность фаготерапии снижается. Ученые обнаруживают такой эффект и в экспериментах над животными, и во время клинических исследований с участием людей. Причем практически невозможно точно измерить, насколько иммунная система мешает фаготерапии. В уравнении с фармакодинамикой фагов, где и без того много переменных, добавляется еще одна.
Сложность №5: риск развития устойчивости к антибиотикам
В некоторых случаях бактериофаги помогают сделать бактерии менее агрессивными или снизить их устойчивость к антибиотикам. Но встречаются и обратные эффекты.

Американский эпидемиолог Стефани Страдти, спасшая своего мужа Томаса Паттерсона от инфекции, вызванной опасной бактерией, с помощью фагов. Это удалось отчасти за счет того, что фаги ослабили возбудителя и сделали его чувствительным к антибиотикам. Подробнее об этой истории – в нашей статье «Бактериофаги плюс антибиотики: убойная комбинация против бактерий». © theperfectpredator.com
Если в фагопрепарате случайно окажутся умеренные фаги, которые встраивают в геном бактерии свою ДНК и существуют в виде профага, то они могут наделить микроорганизмы генами антибиотикорезистентности.
Такая вероятность весьма реальна. Например, исследования показали, что у людей с хроническими и рецидивирующими инфекциями ткани и биологические жидкости буквально нашпигованы бактериофагами, несущими гены антибиотикорезистентности.
Сложность №6: трудности с изучением и регулированием
Главное отличие бактериофагов от большинства других лекарств в том, что это не просто химические соединения, а очень сложно устроенные почти живые биологические объекты. Их взаимоотношения с бактериями и организмом человека многогранны и не изучены до конца. Из-за этого крайне сложно изучать фармакокинетику и фармакодинамику фагопрепаратов, проводить с ними клинические исследования, стандартизировать их.
Большинство упоминаний фагов в научной литературе – это описания одного пациента или небольшой группы. В них не хватает данных, а иногда встречаются и совсем странные наблюдения. Например, больной с бактериальной инфекцией принимает фагопрепарат, ему становится намного лучше, а анализы по-прежнему показывают, что в организме присутствует болезнетворный микроорганизм.
Когда врачи имеют дело с конкретным больным, то часто нельзя однозначно ответить на такие важные вопросы:
- В каких дозах лучше всего вводить бактериофаги?
- Как часто их вводить? Через какие промежутки времени?
- Сколько продолжать курс лечения?
Из-за несовершенства научной базы во многих странах не проработаны вопросы регулирования производства и применения препаратов из бактериофагов. Это создает дополнительные сложности при регистрации таких лекарств.
Несмотря на все недостатки фагов, они всё же работают, – это доказано не раз. Может быть, в будущем ученые смогут разобраться во всех нюансах медицинского применения фагов, и будут составлены четкие протоколы. А пока фаготерапия находит ограниченное применение – нужно отметить, зачастую весьма успешное.
Список литературы и библиографических ссылок:
- gesundheitsindustrie-bw.de – CRISPR/Cas – редактирование генома становится все более популярным
- intechopen.com – Война между бактериями и бактериофагами
- NCBI – Плюсы и минусы фаготерапии
- mdpi.com – Ограничения фаготерапии и соответствующих стратегий оптимизации
- frontiersin.org – Преимущества и недостатки бактериофагов для лечения бактериальных инфекций
- futuremedicine.com – Фаготерапия: неожиданные недостатки
- preprints.org – Показания и ограничения фаготерапии в медицине человека




 Автор на связи, задать вопрос
Автор на связи, задать вопрос